Nicola Barsotti, Diego Lanaro, Marco Chiera
L’eccesso di noradrenalina causa il rilascio di radicali liberi (ROS) che danneggiano il tessuto connettivo, e favorisce l’aumento della produzione di MMP12 (metalloproteinasi) che favorisce il rilascio tissutale di TGF-β1. In questo modo si attiva un binomio estremamente deleterio per la fascia: ROS e TGF-β1, insieme, inducono i fibroblasti a diventare miofibroblasti, cioè cellule dotate di filamenti di α-SMA capaci di rendere il tessuto connettivo contrattile. Va ricordato che tale meccanismo si aggiunge alla stessa stimolazione data della terminazioni nervose del sistema nervoso ortosimpatico.
Chiaramente, in acuto, l’aumento della contrattilità del tessuto è funzionale, ad esempio, aiuta la riparazione di una ferita. Nel cronico, invece, favorisce la formazione di fibrosi (con conseguente produzione citochine infiammatorie), aderenze tissutali e cicatrici sempre più estese e forti: le contratture dei miofibroblasti sono lente, durature e consumano poca energia. Tali contratture generano tensioni meccaniche recepibili dalle integrine di membrana delle cellule del nostro corpo, con conseguente alterazione della biochimica cellulare, attivazione di fenomeni infiammatori e predisposizione alla formazione tumorale.
Vediamo meglio alcuni passaggi prendendo come esempio la riparazione di una ferita.
In acuto l’adrenalina ha due funzioni: rallenta l’attività delle cellule epiteliali e stimola i fibroblasti a proliferare e a dirigersi verso l’area lesa per secernere maggiori quantità di collagene per guarire la lesione.
Finita la reazione di stress, l’abbassamento dei livelli di adrenalina spegne l’attivazione dei fibroblasti, permettendo alle cellule epiteliali di finire la riparazione del tessuto.
In una situazione cronica, l’eccesso di adrenalina ostacola la corretta riparazione: le cellule epiteliali non vanno verso l’area lesa e i fibroblasti non depositano collagene ma rischiano di differenziarsi in miofibroblasti, provocando forti contratture del tessuto attorno alla ferita.
La relazione tra fascia ed ormoni, però non finisce qua. Il sistema miofasciale, infatti, ha recettori per gli ormoni sessuali. Non a caso troviamo recettori per estrogeni nei sinoviociti del rivestimento sinoviale, nei fibroblasti del legamento crociato anteriore, nelle cellule del muro dei vasi sanguigni del legamento.
In vitro, si è visto che l’aggiunta di estradiolo in dosi fisiologiche riduce di oltre il 40% la sintesi di collagene e la proliferazione dei fibroblasti nel legamento crociato anteriore. Inoltre, l’estradiolo, direttamente o indirettamente, tramite la riduzione di IGF-1, inibisce la sintesi di collagene indotta dall’esercizio.
Diventa chiaro, quindi, che è fondamentale chiedere alle nostre pazienti con dolori cronici se fanno uso di terapie ormonali anticoncezionali come la pillola. Sappiamo infatti che gli estrogeni modificano il metabolismo e la struttura del collagene tramite un aumento della lassità legamentosa che si verifica durante la fase follicolare del ciclo mestruale. Inoltre, sempre gli estrogeni Inducono nei fibroblasti la produzione di collagenasi (degrada il collagene) facilitando il prolasso degli organi e la rottura legamentosa. Non è un caso che l’uso di contraccettivi è correlato ad un alto rischio di lombalgia, di fratture ossee, persistente dolore pelvico ed instabilità articolare pelvica.
Iscrivendoti al corso PNEI ed Osteopatia, specifico per osteopati, o La PNEI e il Sistema Miofasciale, diretto a tutti coloro che praticano terapie corporee, avrai modo di approfondire la relazione tra asse dello stress e modificazione della fascia e, pertanto, di avere strumenti efficaci per comprendere meglio la fisiologia e la patologia dei tuoi pazienti.
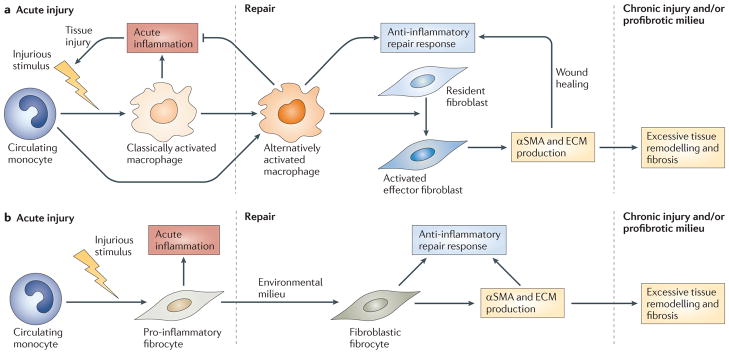
(Fonte immagine: Reilkoff et al. (2011), Fibrocytes: emerging effector cells in chronic inflammation, Nat Rev Immunol, 11(6):427-35.)
Bibliografia
- Barsotti et al. (2021), Impact of stress, immunity, and signals from endocrine and nervous system on fascia, Front Biosci (Elite Ed), 13:1-36.
- Chiera et al. (2017), La PNEI ed il sistema miofasciale: la struttura che connette, Milano, Edra.
- Deo et al. (2013), Norepinephrine increases NADPH oxidase-derived superoxide in human peripheral blood mononuclear cells via beta-adrenergic receptors, J Physiol Regul Integr Comp Physiol, 305:R1124–R1132.
- Goldring et al. (2016) Key components and potential benefits of a comprehensive approach to women’s musculoskeletal health, Physician Sports Med, 7(15):1-9.
- Hansen et al. (2008), Ethinyl oestradiol administration in women suppresses synthesis of collagen in tendon in response to exercise, J Physiol, 586(12):3005–16.
- Liu et al. (1997) Estrogen Affects the Cellular Metabolism of the Anterior Cruciate Ligament, Am J Sports Med, 25(5):704-9.
- Pullar & Isseroff (2005), The beta 2-adrenergic receptor activates pro-migratory and pro-proliferative pathways in dermal fibroblasts via divergent mechanisms, J Cell Sci, 119:592-602.
- Romana-Souza et al (2010), Stress-induced epinephrine levels compromise murine dermal fibroblast activity through beta-adrenoceptors, Exp Dermatol, 20:413–9.
- Wipff & Hinz (2008), Integrins and the activation of latent transforming growth factor beta 1 – An intimate relationship, Eur J Cell Biol, 87:601–15.



Commenti recenti