Francesco Bottaccioli, Anna Giulia Bottaccioli
«L’immunologia, negli ultimi quarant’anni, è progredita con grande rapidità […]. I principi dell’immunologia pervadono la clinica medica. Medici di medicina generale e specialisti, pediatri, chirurghi, ostetrici e ginecologi, neurologi, anestesisti e psichiatri [oncologi, psicologi e neuroscienziati], tutti devono fare i conti con situazioni in cui il sistema immunitario fa sentire i suoi effetti, diretti o indiretti, oppure, al contrario, con disordini che colpiscono l’immunità come conseguenza di una malattia non immunitaria» (Schwartz, 2000, sul New England Journal of Medicine).
Ormai, nessun operatore sanitario e della salute può esimersi dal considerare il sistema immunitario nella sua pratica teorica e clinica. È chiaro infatti che l’infiammazione, sostenuta dal sistema immunitario, condiziona l’evolversi di ogni condizione patologica, ed è persino parte integrante dei disturbi della mente, sia tipo cognitivo-affettivo (psicosi, schizofrenia, disturbo bipolare), sia di tipo umorale (depressione, ansia, disturbo ossessivo compulsivo), sia del neurosviluppo (lo spettro del disturbo autistico) e neurodegenerativo (Alzheimer e Parkinson).
Queste evidenze cliniche sono sorte grazie a decenni di studi che hanno smontato dogmi su dogmi relativi al sistema immunitario: che fosse un sistema chiuso in sé stesso, senza possibilità di comunicare con altri sistemi; che fosse assente nel sistema nervoso centrale, in particolare nel cervello; che le cellule immunitarie avessero un solo fenotipo (ossia possibilità di comportamento) stabile per tutta la loro vita; che gli anticorpi venissero prodotti come meri stampi per semplici antigeni; che l’immunità innata e quella adattiva fossero compartimenti stagni ben distinti; che le cellule immunitarie innate non potessero sviluppare memoria nei confronti di antigeni. Addirittura, è recentissima la scoperta (novembre 2021, Nature Immunology) che le cellule immunitarie innate di un organismo possono non solo creare una memoria immunitaria bensì, tramite meccanismi epigenetici, trasmettere questa memoria alle cellule immunitarie della prole. Insomma, col sistema immunitario non ci si ferma mai di stupirsi!
La ragione di tutte queste scoperte sta nel fatto che il sistema immunitario è estremamente dinamico, ma “equilibrato”, e plastico, al pari se non di più del sistema nervoso.
Il sistema immunitario è infatti in grado di rispondere ai numerosi stimoli che provengono dall’esterno e dall’interno dell’organismo, ma, una volta svolto il compito di intercettare, neutralizzare e memorizzare l’incontro potenzialmente pericoloso, sia esso un microrganismo o una cellula trasformata o una cellula morta, il sistema deve ritrovare il suo equilibrio, che non è mai statico. Il sistema immunitario non è mai spento o fermo: come il cervello, infatti, è sempre attivo e alla ricerca dell’equilibrio.
Come nota Gérard Eberl, capo dell’unità Immunità e microambiente dell’Istituto Pasteur di Parigi, è questa condizione che lo rende pronto a produrre risposte adeguate contro stimoli e minacce di vario genere e, al tempo stesso, a ritrovare il proprio equilibrio dinamico. Tuttavia, se una fonte di stimolo diventa prevalente sulle altre, per esempio se cambia la composizione del microbiota intestinale, oppure l’organismo è esposto a dosi inusuali di tossici ambientali o a condizioni di stress emozionale persistenti, allora l’equilibrio tra i vari circuiti, di cui si compone il sistema, entra in sofferenza, causando alterazioni che porteranno a patologie da disregolazione immunitaria, come le allergie e le malattie autoimmuni, oppure a patologie in cui il sistema immunitario fallisce il suo compito di sorveglianza, come nei tumori, o a patologie alla cui genesi esso dà un contributo di primo piano, come nell’aterosclerosi, nelle malattie cardio-cerebrovascolari, psichiatriche e neurodegenerative.
La scoperta di questo continuo dialogo del sistema immunitario con l’intero organismo e con l’esterno è stata permessa dai ricercatori che hanno seguito le geniali teorizzazioni dello scienziato danese Niels Jerne, il quale ha evidenziato come il sistema immunitario, nel rispondere agli stimoli interni ed esterni, sfrutta una rete di cellule, citochine, recettori antigenici e anticorpi che contestualizzano lo stimolo, il cui significato patogenetico o meno viene attribuito dal contesto più che dalle caratteristiche intrinseche dello stimolo.
Il sistema immunitario, per Jerne, funziona come un network, una rete che è caratterizzata non solo dalla relazione antigene-anticorpo e quindi esterno-interno, ma anche dalla relazione interno-interno e cioè da come un anticorpo viene riconosciuto da altri anticorpi. Per Jerne, un anticorpo può riconoscere ed essere riconosciuto, essere un anticorpo e, al tempo stesso, un antigene per altri anticorpi. La rete, quindi, viene tenuta in equilibrio dinamico da questo complesso sistema di riconoscimenti. Un network che è simile a un altro network biologico, quello nervoso. Jerne stesso paragonò la complessità e la diffusione del sistema immunitario a quella del sistema nervoso. Come il sistema nervoso, il sistema immunitario è costituito da cellule che ricevono segnali eccitatori e inibitori; inoltre, è dotato di memoria.
A tal proposito, «Forse il più interessante progresso concettuale che scaturisce da tutti questi studi è l’idea che la più importante e nuova funzione del sistema immunitario è il suo operare come organo di senso» (Blalock, 1989).
Un organo di senso particolare deputato al riconoscimento di stimoli “non cognitivi” come virus, batteri, tossine al fine di neutralizzarne la potenzialità destabilizzante dell’organismo umano. Come il sistema cognitivo mette in campo diverse funzioni mentali (elaborazione e memoria) e diverse aree cerebrali (visive primarie e diverse aree associative) per “vedere” un oggetto, che non è la sua semplice fotografia bensì la sua elaborazione interpretativa, così il sistema immunitario mette in campo diverse cellule e risponde a una pluralità di stimoli per recepire e interpretare lo stimolo. Il tutto sulla base del contesto (il tessuto, l’organo, il sistema) dove si realizza la ricezione dell’elemento degno di attenzione e il tempo di esposizione.
Un esempio della centralità del contesto è rappresentato dal fatto che l’interleuchina 6 (IL-6) può essere recepita come segnale infiammatorio o, al contrario, come segnale fisiologico, se nel contesto sono presenti o meno altri segnali provenienti da citochine come TNF-α e IL-1. Di regola, infatti, l’IL-6 è associata alla risposta infiammatoria e si trova assieme a un gruppo di altre citochine e mediatori dell’infiammazione, tra cui le citochine sopra menzionate. Situazione tipica è quella causata da un’infezione, che vede le tre citochine tra i primi segnali di attivazione infiammatoria. Tuttavia, anche l’attività fisica, tramite la contrazione muscolare, mette in circolo quantità elevate di IL-6, talvolta addirittura di alcune decine di volte superiori a quelle presenti nel sangue in condizioni normali. Nel contesto dell’attività fisica aerobica e controllata, l’IL-6, invece che attivare una risposta infiammatoria, ne sollecita però una antinfiammatoria riducendo la concentrazione di TNF-α, la cui attività è schiettamente infiammatoria, e stimolando la produzione di altre molecole antinfiammatorie, con effetti positivi su vari sistemi biologici, tra cui il cervello e le funzioni cognitive.
Se vuoi approfondire il funzionamento del sistema immunitario e le sue interazioni in salute e malattia col resto dell’organismo, oltre che le terapie che possono influenzarlo, iscriviti al corso Psiconeuroendocrinoimmunologia, fondamenti fisiopatologici e principi di cura integrata.
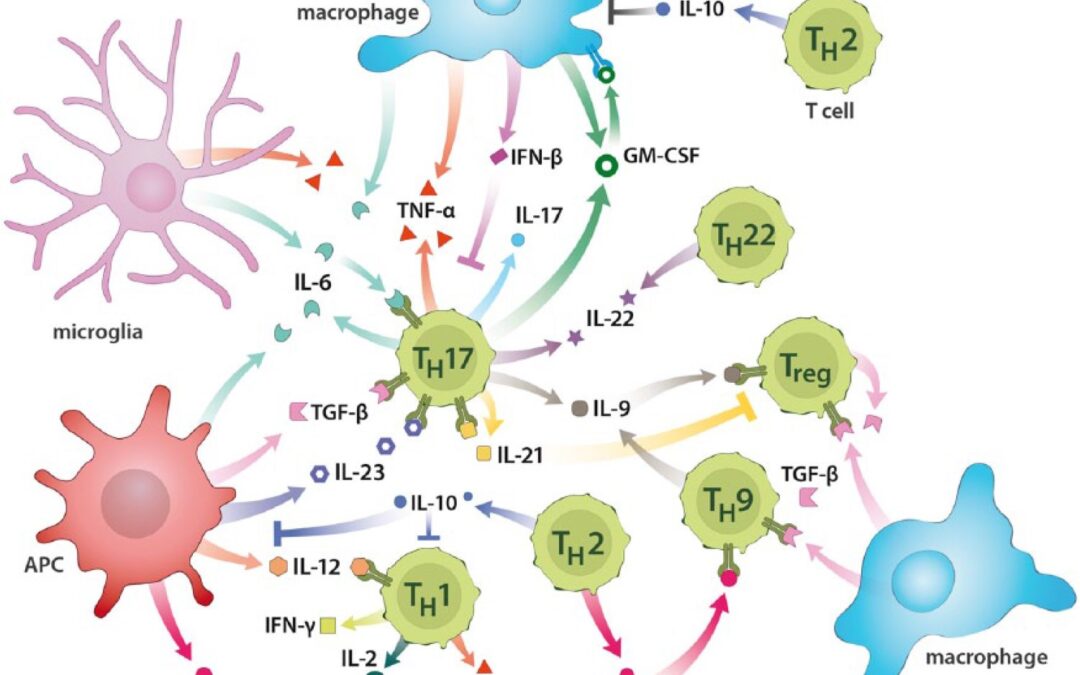
(Fonte immagine: Göbel et al. (2018), Cytokine signaling in multiple sclerosis: Lost in translation, Mult Scler, 24(4):432-9.)
(Tratto da PNEI Review, 1 del 2019)
Bibliografia
- Blalock (1989), A molecular basis for bidirectional communications between the immune and neuroendocrine systems, Phisiol Rev, 69(1):1-32.
- Bottaccioli et al. (2019), Stress and the psyche-brain-immune network in psychiatric diseases based on psychoneuroendocrineimmunology: a concise review, Ann N Y Acad Sci, 1437(1):31-42.
- Bullmore (2019), La mente in fiamme. Un nuovo approccio alla depressione, Torino, Bollati Boringhieri.
- Cronin et al. (2017), The effect of exercise interventions on inflammatory biomarkers in healthy, physically inactive subjects: A systematic review, QJM, 110(10):629-37.
- Gómez-Rubio & Trapero (2019), The Effects of Exercise on IL-6 Levels and Cognitive Performance in Patients with Schizophrenia, Diseases, 7(1):E11.
- Eberl (2016), Immunity by equilibrium, Nat Rev Immunol, 16(8):524-32.
- Jerne (1955), The natural selection theory of antibody formation, PNAS, 41(11):849-57.
- Jerne (1974), Towards a network theory of immune system, Ann Immunol (Inst. Pasteur), 125C(1-2):373-89.
- Jerne (1984), The generative grammar of the immune system. Nobel lecture, 8 December 1984. In: Odelberg, ed. (1985), The Nobel Prizes 1984, Stockholm, Nobel Foundation.
- Katzmarski et al. (2021), Transmission of trained immunity and heterologous resistance to infections across generations, Nat Immunol, 22:1382–90.
- Philippe et al. (2016), Acute effects of concentric and eccentric exercise on glucose metabolism and interleukin-6 concentration in healthy males, Biol Sport, 33(2):153-8.
- Schwartz (2000), Advances in immunology — A new series of review articles, N Engl J Med, 343(1):37-49.
- Tauber (2018), Immunity. The evolution of an idea, Oxford, Oxford University Press.

Commenti recenti