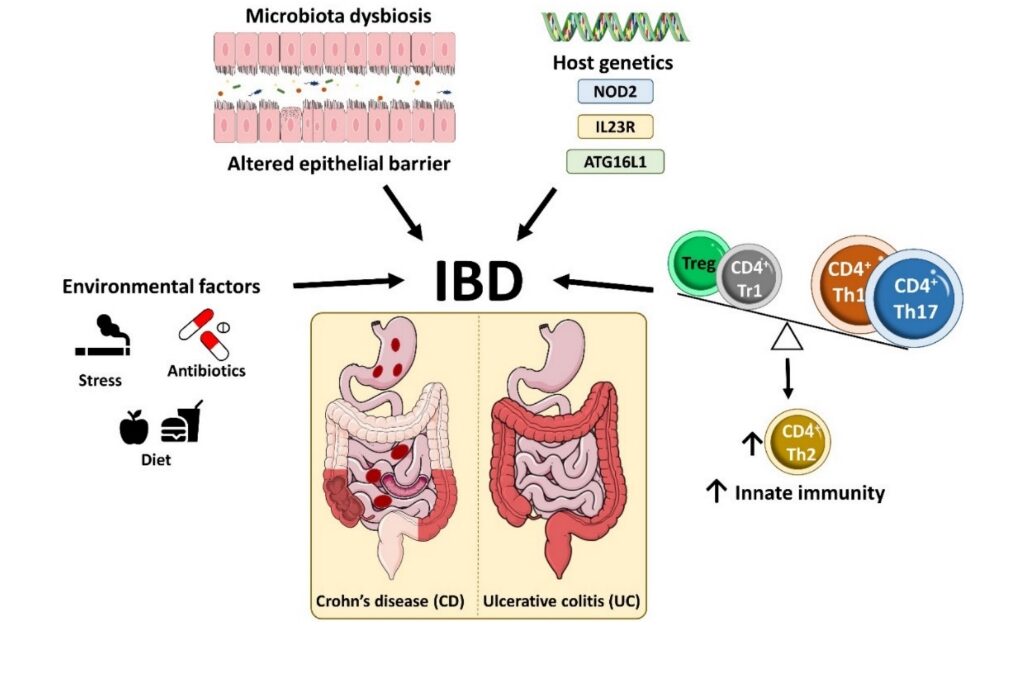
La malattia infiammatoria cronica intestinale (MICI) è una malattia idiopatica autoimmune che produce delle lesioni all’apparato digerente a causa dalla risposta immunitaria disregolata contro la microflora intestinale. I due principali tipi di MICI sono la rettocolite ulcerosa (RCU) e il morbo di Crohn (MC). Diverse sono a tutt’oggi le ipotesi eziologiche. Senza dubbio le tre alterazioni fondamentali riguardano il sistema immunitario intestinale, la barriera intestinale e il dialogo tra sistema immunitario e microflora intestinale. Studi di genetica hanno individuato solamente geni permissivi e non causativi della malattia, lasciando quindi spazio ad una genesi multifattoriale della MICI.
I fattori ambientali (dieta, fumo, pregresse infezioni intestinali, prime fasi della vita) giocano un ruolo importante nella patogenesi, anche se a tutt’oggi non ci sono dati definitivi sul rapporto causale tra un determinato fattore di rischio e lo sviluppo della malattia. L’associazione più consistente ad oggi è quella tra fumo di sigaretta e MC.
Altre associazioni osservate, ma non definitive, sono l’alto introito di fibre da frutta e verdura e la bassa incidenza di MICI, in particolare per il MC, come anche l’alto apporto di proteine animali e di grassi trans (molto diffusi nei “cibi spazzatura” di largo consumo tra i ragazzi) e l’incremento del rischio di malattia infiammatoria intestinale, soprattutto RCU. Confermato il ruolo protettivo degli acidi grassi polinsaturi omega-3 (presenti in grande quantità nel pesce) come fattore dietetico protettivo per RCU. Anche l’aderenza alla dieta mediterranea gioca un ruolo fondamentale nel rischio di malattia. Non a caso, secondo i più recenti dati epidemiologici, l’incidenza globale delle MICI è rimasta stabile in Europa e negli Stati Uniti mentre è cresciuta in Africa, Asia e Sud America, per effetto dell’occidentalizzazione dello stile di vita, in primis alimentare, degli abitanti di questi Paesi.
Inquietante è il dato emerso da una ricerca nazionale condotta sui principali centri ospedalieri di diagnosi e cura delle MICI, in cui oltre il 50% dei pazienti con nuova diagnosi di malattia esce dall’ambulatorio gastroenterologico senza un piano alimentare né consigli su quali cibi preferire e quali evitare.
Le terapie delle MICI e le nuove frontiere di modulazione del microbiota intestinale
La terapia farmacologica delle MICI verte attualmente sull’uso di corticosteroidi ed immunosoppressori (amminosalicilati e DMARDs), di antibiotici per il trattamento di complicanze come fistole ed ascessi e di anticorpi monoclonali anticitochine (farmaci biologici). I dati sul controllo dei sintomi, la remissione della malattia e la prevenzione delle ricadute non mostrano ancora un quadro rassicurante, soprattutto per i quadri patologici di lunga durata. L’intervento di resezione chirurgica di uno o più tratti gastrointestinali resta a tutt’oggi una prospettiva non rara per i pazienti con malattia cronica avanzata, e ad oggi risulta una prospettiva terapeutica altamente invalidante e non scevra da rischi.
Le terapie non farmacologiche: evidenze scientifiche
Di grande interesse risultano quindi gli approcci non farmacologici alle MICI, soprattutto per il loro ruolo prognostico, che andrebbero applicati sin dalle fasi iniziali di malattia, e in presenza di sintomi lievi-moderati (condizione che riguarda i due terzi dei pazienti con MICI) per il controllo della sintomatologia e la prevenzione delle ricadute.
Le terapie non farmacologiche integrate delle MICI iniziano ad avere una letteratura interessante, tanto da aver spinto gli opinion leaders europei in materia a formulare delle linee guida condivise ed evidence-based sui trattamenti di medicina complementare e sulle terapie mente-corpo nelle MICI.
Le terapie mente-corpo, includendo anche l’attività fisica moderata quotidiana, sono oramai entrate a pieno titolo nell’annovero delle terapie non farmacologiche raccomandate delle MICI. Sia la psicoterapia sia la meditazione si sono dimostrate molto utili nell’abbattimento della sintomatologia stressante, nella riduzione delle ricadute di malattia, nel contenimento dei sintomi legati alla riaccensione di malattia e nell’incremento della qualità di vita.
L’uso di probiotici è di comprovato beneficio nel mantenimento della fase di remissione di malattia nella RCU, e l’utilizzo di alcuni preparati brandizzati contenenti delle miscele di Bifidobatteri e Lattobacilli ha ottenuto un alto livello di raccomandazione, anche nella prevenzione delle infezioni della sacca ileale nei pazienti sottoposti ad asportazione di segmenti intestinali per RCU avanzata. Si sta affacciando inoltre la possibilità sempre più concreta di applicare il trapianto di microbiota fecale anche per i pazienti con MICI farmaco-resistente, ad oggi pratica ospedaliera permessa per le sole forme di colite pseudomembranosa infettiva associata ad infezione da Clostridium difficile antibiotico-resistente.
La fitoterapia nella cura delle MICI ha una letteratura fiorente: le ultime metanalisi e revisioni sistematiche hanno mostrato un settore in espansione, con livelli di evidenza sempre maggiori, soprattutto per alcune piante, tra cui la curcuma, fitorimedio dalle proprietà spiccatamente anti-infiammatorie, ad oggi considerata tra le piante più sicure in ambito clinico; seguono l’aloe vera, la Boswellia serrata, l’estratto di Andrographis paniculata, il poliglicoside della Tripterygium wilfordii, la Plantago ovata: tutte si sono tutte mostrate uguali alla mesalazina nel trattamento e mantenimento delle forme di MC e RCU lievi-moderate, senza effetti collaterali importanti.
Un approccio integrato che veda l’essere umano nella sua interezza e che utilizzi tutti gli strumenti a disposizione, farmacologici e non, per aiutare il paziente a gestire la propria malattia, sembra essere ancora una volta la via maestra anche per il trattamento delle malattie infiammatorie croniche intestinali.
Se vuoi approfondire questi argomenti e meglio comprendere la patogenesi e come trattare in ottica integrata le malattie infiammatorie intestinali, iscriviti al corso Psiconeuroendocrinoimmunologia, fondamenti fisiopatologici e principi di cura integrata.
(Fonte immagine: Saez et al. (2021), Innate Lymphoid Cells in Intestinal Homeostasis and Inflammatory Bowel Disease, Int J Mol Sci, 22(14):7618. Licenza CC-BY 4.0)
(Tratto da PNEI Review, 2 del 2020)
Bibliografia
- Ananthakrishnan et al. (2013), A prospective study of long-term intake of dietary fiber and risk of Crohn’s disease and ulcerative colitis, Gastroenterology, 145(5):970-7.
- Ananthakrishnan et al. (2014), Long-term intake of dietary fat and risk of ulcerative colitis and Crohn’s disease, Gut 63(5):776-84.
- Ananthakrishnan et al. (2015), High School Diet and Risk of Crohn’s Disease and Ulcerative Colitis, Inflamm Bowel Dis, 21(10):2311-9.
- Basso et al. (2019), Microbial-Based Therapies in the Treatment of Inflammatory Bowel Disease – An Overview of Human Studies, Front Pharmacol, 9: 1571.
- Brusca et al. (2014), Microbiome and mucosal inflammation as extra-articular triggers for rheumatoid arthritis and autoimmunity, Curr Opin Rheumatol, 26(1):101-7.
- de Mattos et al. (2015), Inflammatory Bowel Disease: An Overview of Immune Mechanisms and Biological Treatments, Mediators Inflamm, 2015:493012.
- Gerbarg et al. (2015), The Effect of Breathing, Movement, and Meditation on Psychological and Physical Symptoms and Inflammatory Biomarkers in Inflammatory Bowel Disease: A Randomized Controlled Trial, Inflamm Bowel Dis, 21(12):2886-96.
- Lam et al. (2019), The Clinical and Steroid-Free Remission of Fecal Microbiota Transplantation to Patients with Ulcerative Colitis: A Meta-Analysis, Gastroenterol Res Pract, 2019:1287493.
- Ng et al. (2018), Worldwide incidence and prevalence of inflammatory bowel disease in the 21st century: a systematic review of population-based studies, Lancet, 390(10114):2769-78.
- Torres et al. (2019), European Crohn’s and Colitis Organisation Topical Review on Complementary Medicine and Psychotherapy in Inflammatory Bowel Disease, J Crohns Colitis, 13(6):673-85e.
- Triantafyllidi et al. (2015), Herbal and plant therapy in patients with inflammatory bowel disease, Ann. Gastroenterol, 28(2):210-20.

Commenti recenti