Nicola Barsotti, Andrea Corti
Emicrania, cefalea e suture craniche in ottica PNEI: perché usare terapie non farmacologiche come osteopatia e agopuntura
Il trattamento di cefalea ed emicrania
Negli ultimi 10 anni, le infiltrazioni dei muscoli pericranici e del collo con l’onabotulinumtossina (BoNT-A) sono state utilizzate regolarmente per il trattamento della cefalea e dell’emicrania cronica (CM). Il problema, però, è che possono verificarsi svariati effetti collaterali come:
- perdita delle rughe della fronte e nella regione glabellare (con conseguente perdita di espressività facciale),
- dolore al collo,
- debolezza muscolare,
- ptosi palpebrale.
Oltre a ciò vi è un ulteriore svantaggio: i costi. Il trattamento con BoNT-A per CM supera i 6.300$ l’anno! Non solo, ogni ciclo di iniezione, da fare ogni tre mesi, prevede 31-37 iniezioni intramuscolari in 7 muscoli della testa e del collo. La procedura, inoltre, è dolorosa poiché il 93% dei pazienti presenta allodinia cutanea.
Il meccanismo fisiopatologico alla base dell’efficacia dell’BoNT-A nella CM non è chiaramente compreso, ma sembra che riguardi il blocco dell’infiammazione neurogenica.
In particolare, sembra che si blocchino una serie di neuropeptidi proinfiammatori, inclusi CGRP e sostanza P, e neurotrasmettitori eccitatori come il glutammato. L’BoNT-A sembra ridurre anche l’attivazione dei canali ionici coinvolti nel dolore come il TRPV1 nelle membrane dei neuroni nocicettivi.
Tuttavia, tali spiegazioni non sembrano bastare. Ecco allora entrare in gioco l’attivazione dei nocicettori meningei internamente al cranio.
Infatti, esistono fibre sensoriali intracraniche, nelle meningi, che inviano rami collaterali capaci di passare attraverso le ossa del cranio e di entrare nel tessuto extracranico attraverso le suture e i canali delle vene emissarie. Tali fibre innervano il periostio e i muscoli extracranici.
È stato a tal proposito dimostrato che l’BoNT-A può inibire la nocicezione meccanica nei neuroni trigeminali periferici nei roditori e che l’iniezione di questa sostanza nella regione della sutura sagittale e lambdoidea può sopprimere la risposta dei nocicettori nella dura madre (l’effetto è più efficace se fatto nella regione vicina alle suture temporali).
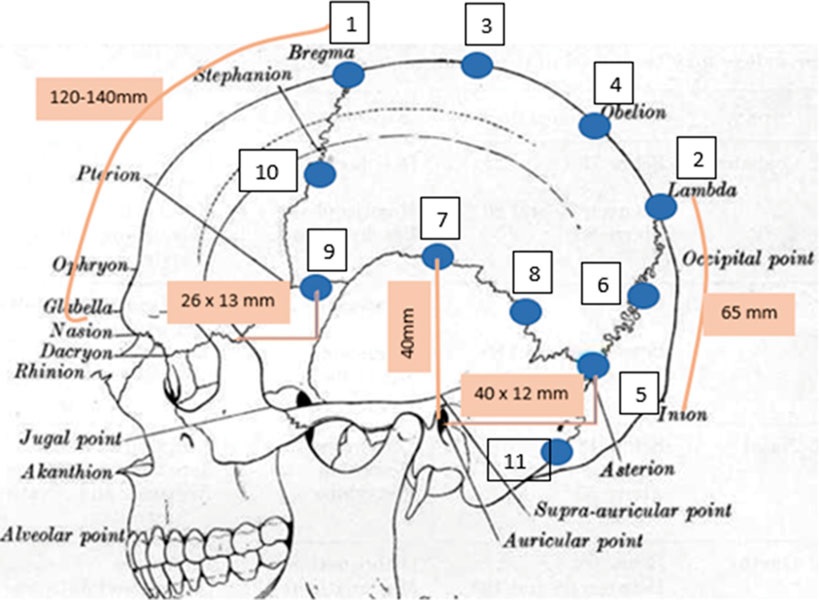
Questi dati suggeriscono che un approccio “follow-the-suture” (FTS) in pazienti con CM potrebbe rappresentare una strategia efficace, meno invasiva ed a minor costo rispetto al paradigma che riguarda il trattamento muscolare.
Queste considerazioni sono particolarmente importanti perché danno un razionale di intervento molto importante per tutte le terapie non farmacologiche della CM come l’osteopatia, l’agopuntura, lo shiatsu e, in senso lato, tutte le terapie manuali. L’osteopatia, in particolar modo, presenta specifiche tecniche per tutte le suture del cranio, per le fasce craniali (come la galea capitis), per il drenaggio linfatico craniale e per le singole fibre nervose extracraniche. I vantaggi di queste terapie sono evidenti: costi estremamente ridotti e assenza degli effetti collaterali che si possono presentare con le infiltrazioni.
Tornando alle suture, studi su topi hanno messo in evidenza come l’innervazione sia particolarmente densa nella regione della sutura occipito-mastoidea e, in particolare, nell’area di inserzione dei muscoli splenio e lunghissimo del capo. Nel cranio umano, si sono evidenziate aree di maggior innervazione a livello della sutura squamosa (tra parietale e temporale).
Nei cuccioli di topo sono stati osservati fasci nervosi che scorrono tra:
- la galea aponeurotica e il periostio;
- il periostio e l’osso;
- l’osso e le meningi;
- vi sono fibre che scorrono anche all’interno del diploe (è lo strato di tessuto osseo spugnoso ben vascolarizzato, posto tra i tavolati esterno e interno delle ossa piatte del cranio) e che presentano orientamenti diversi;
- alcune fibre durali mandano rami collaterali alla pia madre nella parte frontale del cervello.
Nel cranio degli adulti, la più alta concentrazione di fibre, che sembrano emergere dalla dura madre, è stata trovata:
- nelle suture,
- nei canali emissari,
- nel midollo osseo,
- nel periostio.
I nervi meningei che si infiltrano nel periostio, passando attraverso le suture craniche, possono attivare la nocicezione nei tessuti extracranici (muscoli e fasce) e quindi favorire dolore. Piccoli traumi, pertanto, possono essere fonte di stimolazione delle suddette fibre. Non solo, i ricercatori dicono che, data la concentrazione di fibre sensoriali nelle suture, potrebbe essere utile evitare di perforarle nei pazienti sottoposti a craniotomia durante le procedure neurochirurgiche.
Approfondimento sull’innervazione pericranica e durale trigeminale nella regione parieto-temporale
La patogenesi della cefalea, in particolare quella primaria come l’emicrania, è ancora lungi dall’essere chiara. Per cercare di fare un po’ di luce sulla fisiopatologia che può generare la cefalea è utile fare un approfondimento dell’innervazione in queste aree.
Dal punto di vista fisiologico, il nervo principale della fossa cranica media è il nervo spinoso, che deriva dal V3. Questo nervo accompagna l’arteria meningea media (AMM) e si divide in quattro o cinque rami principali. Uno di questi rami corre verso la fessura petrosquamosa dividendosi in due rami più piccoli. Tutti gli altri rami vanno in direzione parietale o rostrale seguendo l’AMM. Questi fasci nervosi si dividono in fasci più piccoli, alcuni dei quali incrociano mentre altri accompagnano i rami arteriosi. Alcune fibre nervose si staccano dai fasci e decorrono nell’avventizia dell’AMM. Altri rami, invece, decorrono nel tessuto connettivo durale e si arborizzano in modo dicotomico prima di terminare. Seguendo questo schema di innervazione, l’intera dura parietale e temporale presenta una fitta rete di fibre nervose.
Da mettere in evidenza che le fibre nervose del nervo spinoso non sono presenti nel seno sagittale superiore, nel seno trasverso, nel tentorio cerebellare, nella fossa cranica frontale e occipitale.
Lungo il percorso nella fossa cranica media, fasci di fibre nervose decorrono lungo l’osso ed entrano, in particolare, nelle aperture intracraniche delle venule emissarie e nelle suture tra:
- l’osso parietale e frontale,
- l’osso temporale e l’osso parietale,
- l’osso temporale e l’osso occipitale.
Le fibre fibre nervose del nervo spinoso escono quindi dal cranio. Questi fasci, una volta che si trovano sulla parte esterna della nostra testa, decorrono trasversalmente lungo la volta cranica, mentre singole fibre si diramano e terminano nel diploe.
Parte dei rami che decorrono nella fessura petrosquamosa:
- attraversano anche la sutura lambdoidea,
- o corrono all’interno dell’osso in direzione occipitale,
- o corrono lungo la vena facciale posteriore e la vena mascellare interna in direzione caudale.
Dagli studi, i ricercatori stimano che circa il 10-20% delle fibre meningee del nervo spinoso lasciano il cranio seguendo la traiettoria descritta. In questo modo si formano circa 10 fasci su ciascun lato con assoni mielinici e amielinici.
La proiezione extracranica delle fibre nervose è variabile ma segue uno schema di base. I fasci nella fessura petrosquamosa, come abbiamo visto, lasciano il cranio o attraverso la sutura lambdoidea tra l’osso temporale e quello occipitale, o dopo aver seguito un percorso più lungo all’interno della cresta nucale occipitale.
Le fibre nervose entrano nel periostio extracranico e scorrono in stretta vicinanza ai vasi sanguigni arteriosi, emettono piccoli rami e formano una rete periostale di fibre trigeminali simile a quella della dura madre.
Infine, la maggior parte di queste fibre nervose attraversa il periostio ed entra nelle giunzioni tendinee dei muscoli pericranici, in particolare nel muscolo temporale. Un’innervazione particolarmente densa si trova negli attacchi dei muscoli nucali superiori, cioè lo splenio ed il longissimus capitis, dopo che le fibre hanno lasciato il cranio lungo la cresta nucale tra l’osso temporale e quello occipitale.
Alcune fibre trigeminali si diffondono in profondità nei compartimenti del tessuto connettivo dei muscoli pericranici, dei muscoli masticatori, di quelli della parte superiore del collo e persino tra le fibre muscolari stesse.
Sorprendentemente, una parte considerevole delle fibre nervose che lascia il cranio caudalmente a livello della cresta sopramastoidea, si trova nella capsula e nel connettivo dell’articolazione temporo-mandibolare.
È anche interessante notare che, nella regione nucale, il territorio di innervazione del trigemino sembra sovrapporsi al territorio dei nervi occipitali (è stato dimostrato che le fibre nervose extracraniche in questa regione non sono di origine spinale perché la colorazione era completamente assente nei nervi occipitali).
Ecco quindi trovata una relazione importante tra ATM, innervazione trigeminale, sensitizzazione centrale trigeminale, attivazione dell’asse dello stress, emozioni, infiammazione, modificazione della densità fasciale cranica, biomeccanica dell’ATM!
Forse, quindi, considerare la relazione postura-occlusione solo nell’ottica biomeccanica-posturale è un “tantino riduttivo”, e questa è solo l’ennesima conferma di come questo paradigma sia superato e, come riportiamo da anni, non confermato clinicamente dalla ricerca.
La conseguenza è il bisogno di una pratica clinica che consideri il paziente nella sua complessità.
In quanto medici, osteopati o professionisti della salute, diventa pertanto essenziale affrontare la cefalea, soprattutto se cronica, da molteplici punti di vista in modo da giungere a capire – e a far capire al paziente – quali sono gli stimoli che maggiormente stanno influenzando il quadro clinico del paziente.
Solo così si può attuare una terapia mirata ma soprattutto efficace.
Finiamo l’approfondimento sull’innervazione pericranica e durale trigeminale nella regione parieto-temporale sviluppando due ulteriori argomenti:
- il ruolo delle fibre mieliniche e amieliniche del nervo spinoso,
- il ruolo del ganglio del trigemino e le proiezioni centrali.
Per quanto concerne il primo punto, possiamo iniziare dicendo che le fibre nervose mielinizzate riscontrate in queste aree sono Aβ. Sono fibre capaci di assorbire normalmente le funzioni meccano-recettive e, sembra, anche quelle nocicettive (es. dolore evocato dalla stimolazione della dura madre durante gli interventi chirurgici alla testa). È stato ipotizzato anche che queste fibre nervose possano essere attivate da stimoli meccanici come quelli generati dai movimenti improvvisi della testa. Questa idea è particolarmente interessante per quanto riguarda il loro possibile contributo all’emicrania e alla cefalea cronica di tipo tensivo.
Inoltre, l’innervazione dei muscoli esocranici con fibre nervose mielinizzate potrebbe essere data non solo dai collaterali delle afferenze meningee, ma anche da fibre propriocettive che viaggiano attraverso il ganglio trigemino per finire nei loro somi situati nel nucleo mesencefalico trigeminale.
Comunque, mentre il ruolo delle fibre Aβ nella nocicezione meningea non è chiaro, è molto probabile che le fibre Aδ e C (parzialmente mielinizzate o amieliniche) penetranti nel cranio, dato che sono nocicettive, siano coinvolte nella generazione del mal di testa.
Se colleghiamo a questa informazione il fatto che l’osteopatia agisce sulla stimolazione delle fibre C, si può avere un ulteriore razionale per spiegare l’efficacia dell’OMT in pazienti cefalalgici.
Ricordiamoci infatti che le fibre C, nella loro enorme varietà, mediano il tocco nelle sue più varie sfaccettature: se negli ultimi anni è emerso il legame fra le fibre C-tattili e il tocco gentile, è anche vero che anche pressioni profonde attivano le fibre C. E allo stesso modo, anche terapie manuali più “strong” quali manipolazioni spinali o thrust attivano alcune particolari fibre C, tra l’altro favorendo meccanismi opposti alla sensitizzazione e, quindi, favorendo l'”oblio” delle sinapsi formate in caso di trauma. Inoltre, nel momento in cui il paziente viene posto al centro della terapia come “partecipante attivo”, lavori sul corpo quali trattamenti osteopatici, di psicoterapia a base corporea, etc. possono favorire l’attivazione dei network nervosi centrali (es. il central autonomic network) che stanno a capo dell’attività neurovegetativa e interocettiva e, quindi, a capo dello stato di attivazione delle fibre C e dei nervi cranici coinvolti nella regolazione autonomica.
A conferma di quanto appena detto, riportiamo le testuali parole dell’articolo di riferimento: “potrebbe spiegare perché le terapie manuali delle strutture pericraniche possono avere successo nella gestione del mal di testa”.
Non si può poi escludere che le fibre nervose che corrono con o parallelamente al nervo spinoso abbiano un’origine simpatica o parasimpatica e contribuiscano alle funzioni vascolari.
Riguardo il secondo punto, possiamo dire che i ricercatori hanno studiato anche le vie nervose che dal nervo spinoso vanno i nuclei trigeminali. Nelle loro ricerche è emerso che i corpi cellulari delle fibre trigeminali del nervo spinoso si trovano esclusivamente nel V2 e V3 del ganglio del trigemino e, in questo, più del 70% dei neuroni è localizzato nella parte posterolaterale del V3.
Seguendo il percorso verso i nuclei trigeminali, si è visto che queste fibre originano:
- nel nucleo del trigemino spinale: è uno dei 4 nuclei di origine di questo nervo ed è situato nel midollo allungato. È un nucleo sensitivo e contiene principalmente i neuroni adibiti al trasporto degli impulsi tattili più grossolani e termonocicettivi. È interessante notare che riceve anche fibre sensitive dal glossofaringeo e dal vago;
- nel subnucleo interpolare e caudale sempre del nervo spinale: fibre nervose che innervano i vasi sanguigni cranici, intracranici (AMM, seno sagittale superiore) o extracranici (arteria temporale superficiale).
È noto che il nucleo del trigemino spinale è principalmente coinvolto nella trasmissione di informazioni nocicettive dall’interno e dall’esterno della testa e del viso. È interessante notare, al fine della nostra clinica osteopatica, che non è stata identificata una separazione spaziale della trasmissione nocicettiva intra ed extracranica. Tutto questo sottolinea l’idea che l’input afferente, sia esso intracranico o extracranico, può contribuire alla generazione di mal di testa.
Se ti interessa approfondire come poter agire sui nervi cranici e sulle varie vie afferenti coinvolte nella cefalea, nell’emicrania così come in altre situazioni dolorose, acquista il corso L’odontoiatria incontra l’osteopatia II livello – Il dolore oro-facciale.
(Fonte immagine: Stovner et al. (2022), FollowTheSutures: Piloting a new way to administer onabotulinumtoxinA for chronic migraine, Cephalalgia, 42(7):590–7.)
Bibliografia
- Kosaras et al. (2009), Sensory innervation of the calvarial bones of the mouse, J Comp Neurol, 515(3):331–48.
- Schueler et al. (2014), Innervation of rat and human dura mater and pericranial tissues in the parieto-temporal region by meningeal afferents, Headache, 54(6):996–1009.
- Stovner et al. (2022), FollowTheSutures: Piloting a new way to administer onabotulinumtoxinA for chronic migraine, Cephalalgia, 42(7):590–7.

Commenti recenti